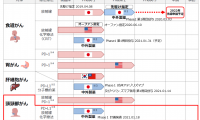
こんにちは、シエン(@m12n08.jp)です。

【本ページは2019年4月に書いた記事を2021年1月に加筆しました】
2019年12月30日(月)時点で4588オンコリスを15,500株保有しています(平均取得価格約2,035円)。
もしオンコリスの株価が30,000円になれば私の株資産は4.65億円となります。
なることは間違いないと個人的に思っており、問題は「いつか」ということです・・・。
さて、今後どのようになっていくでしょうか。
今後、ブログにオンコリスの将来性について書いていきます。
4588オンコリスバイオファーマの直近業績推移(2020年6月時点)

2020年6月13日(土)時点の日経新聞(WEB)に掲載されている4588オンコリスバイオファーマの2020年12月期の売上予想は700百万円、税後利益▲500百万円(赤字)となっています。
まだ上市(薬が市場販売されること)された薬のないオンコリス社は赤字の創薬バイオ企業ですが、その将来性は「Google × Amazon」級のポテンシャルがあると私は考えています。
世の中には「赤字会社の株は購入しない」「マザーズの株は買わない」という方も多いのは事実ですが、赤字・マザーズ上場という理由だけで株式投資先からオンコリスを検討対象外とするのは勿体ないと思います。
中外製薬への独占的ライセンス契約および資本提携契約(2019年4月)
オンコリス社は2013年にマザーズに上場しました。
資本政策で、これまで一番のビックディールは、何といっても2019年4月8日に適時開示された「中外製薬へのOBP-301(テロメライシン)の導出と、資本提携契約」です。
オンコリスバイオファーマ株式会社(以下、「オンコリス」)と中外製薬株式会社(以下、「中外製薬」)は、このたび、オンコリスが開発中のがんに対するウイルス療法である「テロメライシン(OBP-301)」(以下、「テロメライシン」)について、日本・台湾における開発・製造・販売に関する再許諾権付き独占的ライセンスを中外製薬に付与すると共に、日本・台湾・中国・香港・マカオを除く全世界における開発・製造・販売に関する独占的オプション権を中外製薬へ付与するライセンス契約を締結しました。
中外製薬は、日本・台湾における再許諾権付き独占的ライセンス契約の契約一時金として5.5 億円を支払います。また、テロメライシンの臨床試験において一定の効果が確認され、中外製薬が上記の独占的オプション権を行使した場合には、中外製薬がオンコリスに支払う本ライセンス契約総額は500 億円以上になります。さらに、テロメライシンの上市後は、中外製薬におけるテロメライシンの売上額に応じた販売ロイヤリティを、ライセンス契約総額とは別に、中外製薬がオンコリスに支払います。
出展:がんのウイルス療法「テロメライシン(OBP-301)」に関する 独占的ライセンス契約および資本提携契約の締結について
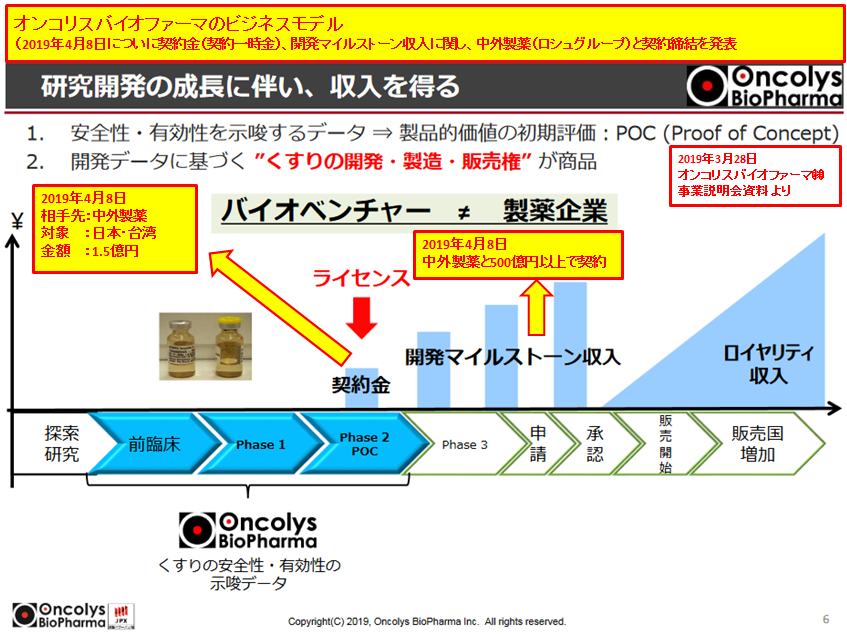
オンコリスはこの導出以後は、日本における治験は中外製薬が実施することとなりました(2021年1月時点で国内 食道癌 第二相治験中)。
上市品がないバイオベンチャーにとって治験を進めるための費用支出は重荷ですが、OBP-301(テロメライシン)の日本国内治験費用を負担しなくてよくなることは資金繰りに取っては非常に大きなアドバンテージとなります。
しかしそれでもオンコリスは海外での治験も進めていますので今後も資金は年間5~10億円単位で必要となります。しかし中外製薬は「再許諾権付き独占的ライセンス」を持っており、海外については将来的には中外製薬の株主である世界のロシュへ導出が期待されています。
ホルダーとしては2020年末まで、遅くとも2021年半ばにロシュが中外製薬の再許諾先となると期待しています。
結果、Quickコンセンサスでは既に1社が売上高と当期利益の訂正を行っており、会社発表はまだですが2019年12月期は税後▲4億円(2018年は▲12億円)となる見込みであり税後で8億円の大幅改善となる予定です。
 金額の多寡というよりも、あの中外製薬がオンコリスの創薬事業が順調に進んでいることを認めていることが非常に意義高いことと思います。
金額の多寡というよりも、あの中外製薬がオンコリスの創薬事業が順調に進んでいることを認めていることが非常に意義高いことと思います。
また上市へ確実に進んでいることを意味しており、抗癌剤の副作用に苦しむ患者さんにとっても希望の光が大きく輝きだしたと言えます。
先駆け審査指定制度とオンコリス テロメライシン®
既にご存じの方は多いと思いますが、2019年4月にオンコリスのがんのウイルス療法テロメライシンⓇ(OBP-301)は「先駆け審査指定制度」の対象品目に指定されました。参考まで厚生省HPで発表されている「先駆け審査指定制度」の具体的なイメージ図を掲載します。
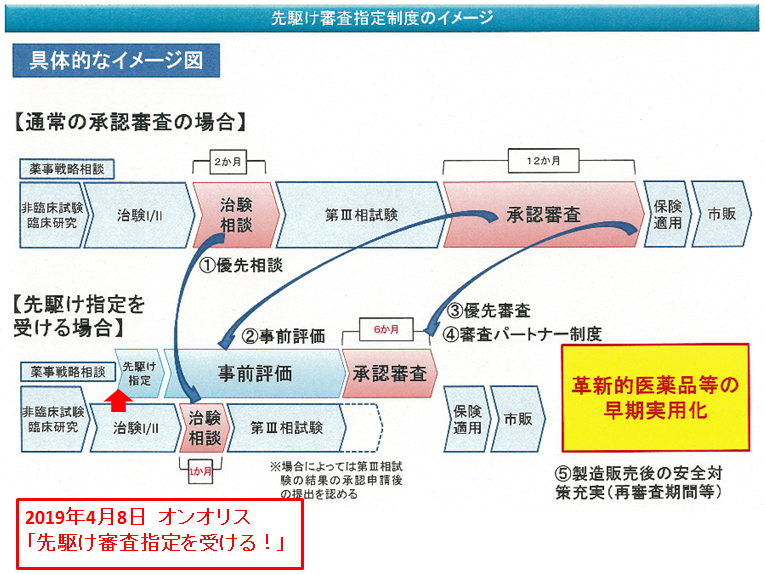
「先駆け審査指定」を受けたことで、通常は第三相試験後に行う「事前評価」を第二相治験が終了したタイミングで出来ることになります。ポイント箇所を拡大して説明します。

よって通常12ヶ月必要とされている承認審査が半分の6ヶ月となります。
これは1日も早く上市されることを待っている癌患者にとっては、自身への保険適用によるOBP-301(テロメライシン®)の投与が半年早まることを意味しており大変意義高いものとなります。
4588オンコリスバイオファーマの将来の株価予想(2019年5月時点)

さて、2019年5月1日時点で私が見据えている4588オンコリスバイオファーマの将来の予想株価(希望株価)ですが次の通りです。「いつそうなるの?」と問われても私は素人なので答えられません。このブログで書いていることは、あくまでも私の希望であり予想です。オンコリスの株式を購入する場合、投資判断は自己責任でお願いします、当ブログ管理者として責任は一切負えません。

<前提>発行済株式数 14,205,100株(2019年4月24日第三者割当増資考慮後)
【EPS 352円、PER100倍計算】
税後純益 5,000百万円/年(2023年末)
EPS(1株利益)352円/株
PER 100倍
理論株価 約35,000円/株
【EPS720円、PER 200倍】
税後純益 10,000百万円/年(2025年末頃?)
EPS(1株利益)704円/株
PER 200倍
理論株価 約140,800円/株
収益に貢献するものは次の2点です。
①適時開示されたライセンス契約総額(500億円以上)
②テロメライシン(OBP-301)の上市後、テロメライシン(OBP-301)の売上額に応じて中外製薬からオンコリスへ支払われる販売ロイヤリティ(金額不明)
PERに関しては、バイオ分野に限らず成長著しいベンチャーであれば将来の増益を見込んでPER100倍、PER200倍となることも珍しくありません。
まぁ、上述数字はオンコリス現物株を握る私自身の握力を高めるため意図的にかなりポジティブに書いています(笑)
さて、株価が飛躍的に上昇するチャンスは「赤字から黒字に転換するポイント」です。毎年10億円以上の赤字を続けているバイオベンチャーが、令和元年から飛躍する今こそ、私は現物株を握りしめて長期目線で応援したいと考えています(2021年に株価暴騰がやってくると期待しています)。
【2020年6月13日追記・訂正】
2020年3月より国内の10施設以上で食道癌第二相治験が始まりました。
今後はオンコリス社が開発している腫瘍溶解性ウイルス「テロメライシン」の評価が、まずは病院関係者の間で話題となってくるはずです。
知り合いに癌治療に携わられているお医者様がいらっしゃる方は是非、質問されてみて下さい。4588オンコリスの革命的な薬効に気づくはずです。
オンコリスの飛躍可能性が格段に高まった中外製薬(ロシュグループ)との業務提携

2019年2月12日の社長コラムに次のようにコメントがあります。
「更に最近になり,乳がん,頭頸部がん,咽喉がん,肺がん,骨肉腫,尿管がんなど,多岐にわたるがん種に対してテロメライシンで臨床試験を実施したいという国内外からの申し出があり,弊社としては嬉しい悲鳴が上がっています。」
これまで毎年10億円以上の税後赤字を継続しているオンコリスとしては、バーンレート(会社を経営していくために1ヶ月 or 1年にいくらの資金が必要になるかという指標。 資本燃焼率とも言われる。)を気にしながらの会社運営となっていました。
しかし、今回、ガン領域で国内トップである中外製薬と提携出来たことで、資金並びにネットワークの制約から取り組めなかった各種ガン「乳がん,頭頸部がん,咽喉がん,肺がん,骨肉腫,尿管がん」に対してもテロメライシンの臨床試験件数を数倍以上に加速させながら実施できる財政的基盤を確保したと言えると思います。

上の資料は中外製薬が2019年4月に発表した1Q資料です。
「ガンを溶かし、正常な細胞の中では増殖能力が極めて低い」という画期的なガン治療薬となる期待がテロメライシンには期待されています。
世界中でテロメライシンを使用して、乳がん,頭頸部がん,咽喉がん,肺がん,骨肉腫,尿管がんの治験が開始されるのは時間の問題であり、ひょっとすると2019年5月10日のオンコリス社の1Q業績発表時に何か報告・発表があるかもしれないですね。現物株ホルダーとしてはどうしても期待してしまいます。(⇒結論としては2020年3月3日に食道癌 治験第二相が日本国内で開始されるに至りました!)
4588オンコリスバイオファーマの将来の株価予想(2021年1月時点)

さて2019年4月の初めてオンコリスの株についてブログ記事を書いてから9ヶ月が経過しました。その後、国内外の治験も進展があり、また個人投資家向けの説明会で浦田社長自ら今後の事業進展時期などを口頭説明して下さっています。
主だった期待される事業進展についてまとめたものが上述表です。
本当は中外製薬やハンルイ(中国)からのマイル収入はもう少し多く発生すると思っているのですが、そこは割り引いて表に落とし込んでいます(2020年6月13日追記:ハンルイとの中国・香港・マカオの独占的ライセンス契約は2020年6月9日に解消されました。 プレスリリース「テロメライシンのハンルイ社との提携解消について」)。
これは私(シエン)が個人的に期待している株価期待値です。実際、どのようになるか個人で楽しむものであり、記載内容に事実誤認が含まれている可能性があります。
各イベントは各自がオンコリス社が発表している1次情報から確認の上、投資は自己責任でお願いします。
では本日のブログは、厚生省の「先駆け審査指定制度」について簡単にまとめて終わりとさせて頂きます。
【参考】先駆け審査指定制度とは

「先駆け審査指定制度」は、世界に先駆けて、革新的医薬品・医療機器・再生医療等製品を日本で早期に実用化すべく、世界に先駆けて開発され、早期の治験段階で著名な有効性が見込まれる医薬品等を指定し、各種支援による早期の実用化を目指すため2015年4月1日に創設された制度です。
「先駆け審査指定制度」の対象品目として、オンコリスのがんのウイルス療法テロメライシン(OBP-301)は、2019年4月に指定されました。
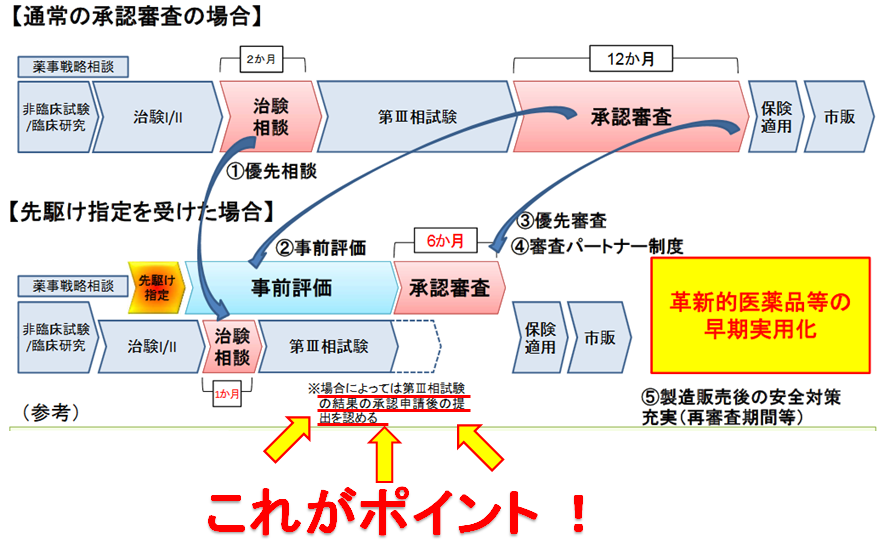
再掲となりますが、ポイントは、今後第三相試験の結果を承認申請後の提出で良いとされる可能性があるということです。これにより承認審査に速やかに入ることが出来、保険適用・市販(上市)までの時間が大幅に短縮されることになります。(中外製薬は同社のプレスリリースでOBP-301テロメライシンの申請時期は2022年と公表しております)→ 中外製薬 2020年第1四半期決算説明資料

4588オンコリスバイオファーマ/2013年上場時の浦田社長インタビュー